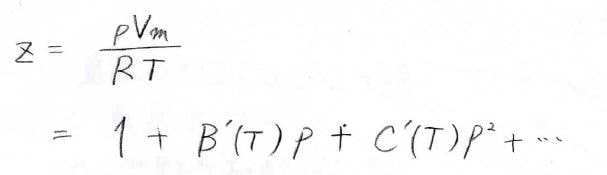圧縮率因子(あっしゅくりついんし、英: compressibility factor)は実在気体の振る舞いに関して、理想気体からのずれを表す無次元量のひとつである。圧縮因子あるいは圧縮係数ともいう。
実在気体または理想気体について、P、V、n、T をそれぞれ圧力、体積、物質量、温度とすると、圧縮率因子 z は次のように表される。
ここで R は気体定数である。また、Vm は気体分子のモル体積、 Vmideal は理想気体としてプロットしたモル体積である(便宜上、前者をモル体積、後者を理想のモル体積と呼ぶことにする)。
モル体積と理想のモル体積の商をビリアル展開することでz を求める方法もある(詳細はビリアル方程式を参照)。
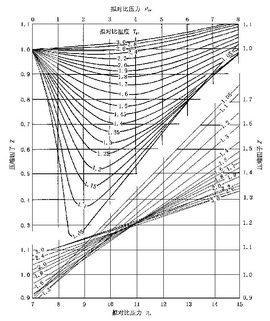
z は圧力 P に対してプロットすると物質固有の曲線になる。一般に十分低圧では1より小さく、十分高圧では1より大きくなる。これは実在気体では無視できない分子間力と分子自体の体積の2つの影響によるものである。z を対臨界定数P およびT の関数で表したのがz 線図で、気体の種類に関係なく適用できる。
理想気体では
より圧縮率因子の値は常にz = 1である。
空気の圧縮率因子
参考文献
- McQuarrie, Donald A. and Simon, John D. (1999). Molecular Thermodynamics. University Science Books. ISBN 1-891389-05-X. page 55
- Perry's chemical engineers' handbook (6ed ed.). MCGraw-Hill. 1984. ISBN 0-07-049479-7. page 3-268
- Smith, J.M. et al. (2005). Introduction to Chemical Engineering Thermodynamics (Seventh Edition ed.). McGraw Hill. ISBN 0-07-310445-0. page73
関連項目
- 実在気体
- ファンデルワールスの状態方程式
- ディーテリチの状態方程式
- 圧縮率